肉芽肿是免疫细胞在各种器官形成的肿块。大多数肉芽肿看起来没有结构,但它们与淋巴器官有一些相似之处。为了更好地理解肉芽肿的形成,本文对结节病患者的肉芽肿进行了原位单细胞精准定量和空间转录多组学分析,并用生物信息学方法重建了潜在的基因调控网络。
2023年2月14日,维也纳医科大学的Georg Stary团队在Immunity(IF=43.5)上发表了题为 “Single-cell and spatial transcriptomics reveal aberrant lymphoid developmental programs driving granuloma formation” 的研究论文。
本文发现肉芽肿中存在一个免疫刺激性环境,它重新利用了与淋巴器官发育相关的转录程序。肉芽肿的形成遵循特征性的空间模式,并涉及与免疫代谢、细胞因子和趋化因子信号传导、细胞外基质重塑相关的基因。我们确定了三种在肉芽肿形成中起关键作用的细胞类型:代谢重编程的巨噬细胞、产生细胞因子的Th17.1细胞和具有炎症和组织重塑表型的成纤维细胞。结果表明,人类肉芽肿采用了正常淋巴器官发育中具有特征性的方面,但以异常的组合方式出现构成了异常的淋巴器官。
实验部分
本文使用TissueGnostics公司TissueFAXS全景组织细胞定量分析系统获取免疫荧光图像。获取到图像利用TissueQuest软件进行定量分析。
在本文中,研究者针对TissueQuest的精准识别原理做了详细的说明。


为了研究持续性皮肤结节病患者肉芽肿(Granuloma,GA)相关细胞亚群,研究者在冰冻皮肤切片中使用免疫荧光蛋白染色技术,利用DAPI标记细胞核,CD68、CD3和CD90作为细胞类型定义的表面标记,定位真皮巨噬细胞、T细胞和成纤维细胞。在此基础上,获得的图像被导入TissueQuest中。在软件中,病变性皮肤切片被分为表皮和真皮区域,只有真皮区域被包含在最终分析中,去除了表皮区域;同时为了避免高自发荧光信号的干扰,大汗腺及其周边区域也做了额外的组织去除。
在单细胞精准识别的阶段,使用DAPI通道先对细胞核进行识别,排除细胞碎片和黏连细胞;之后根据单细胞不同通道的染色面积,TissueQuest软件使用核扩张算法分割了每个细胞的真实染色轮廓。根据真实轮廓内的染色强度和染色面积,设置相同的散点图Cutoff阈值来确定信号强度,将细胞识别为“阳性”或“阴性”。
在组织识别阶段,将肉芽肿结构定义为具有一定形态且紧密的细胞聚集体,内部有密集的CD68+巨噬细胞,其外周有强阳性信号的CD90+成纤维细胞,T细胞散布在巨噬细胞和成纤维细胞之间。继而将目标定量的真皮部分进一步分为两组:第一组包括含有肉芽肿的真皮区域,第二组包括不含肉芽肿的真皮区域。这些区域在组织原位彼此靠近,研究者使用肉芽肿外层成纤维细胞作为各自的亚分类线。每个真皮亚组输出以下参数:每平方毫米的细胞数、感兴趣标记的平均强度(详见各自图例)和父群体的相对百分比。
巨噬细胞、T细胞和成纤维细胞是皮肤肉芽肿的主要细胞类型
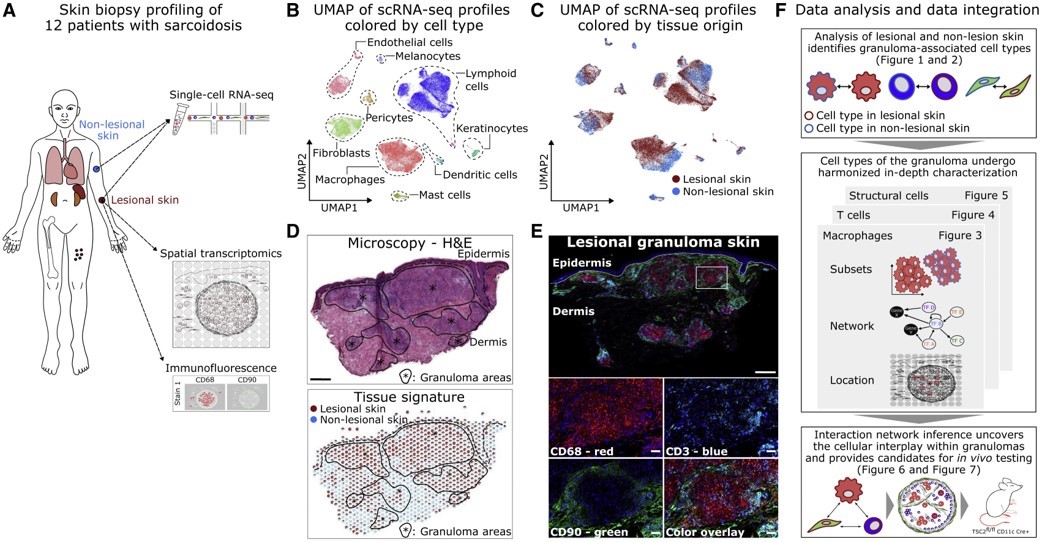
Figure 1. 巨噬细胞、T细胞和成纤维细胞是皮肤肉芽肿的主要细胞类型
(E)皮肤肉芽肿的免疫荧光样本图像:巨噬细胞CD68(红色;APC)、T细胞CD3(浅蓝色;PE-TR)、成纤维细胞CD90(绿色;FITC)和DAPI细胞核(深蓝色)。
GA巨噬细胞表现出强烈的促炎性特征
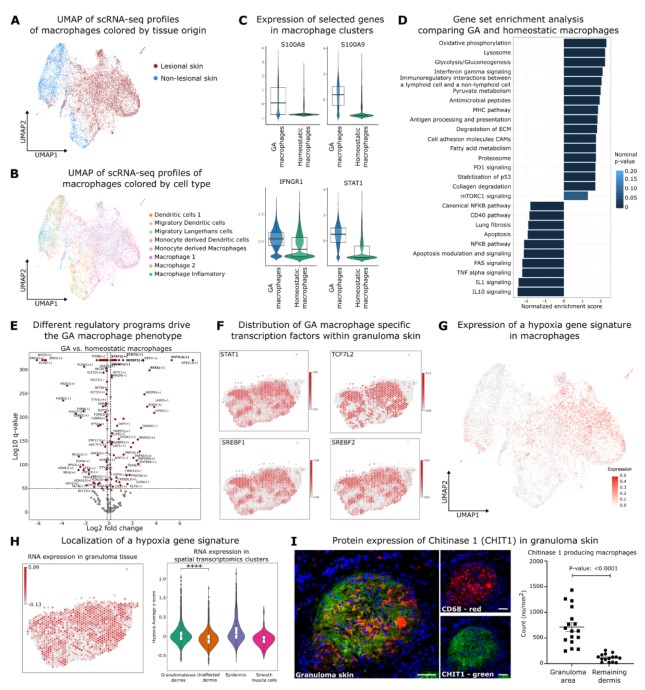
Figure 2 GA巨噬细胞形成的肉芽肿内部存在高度炎症环境。
(I)免疫荧光样本图像表明皮肤肉芽肿中的几丁质酶 1(CHIT1,绿色;AF488)、CD68(红色;APC)和 DAPI(深蓝色)。
左:一例结节病肉芽肿结构的荧光图像。右:几丁质酶 1 表达的巨噬细胞(CD68+CHIT1+)的定量分析免疫荧光染色样本结果证实了GA0巨噬细胞在肉芽肿中特异性表达几丁质酶1(Figure 2I)。
TissueQuest这些巨噬细胞支持适应性免疫反应和ECM重塑,从而有助于肉芽肿中持续炎症的微环境。
具有Th17.1表型的T细胞富集在肉芽肿
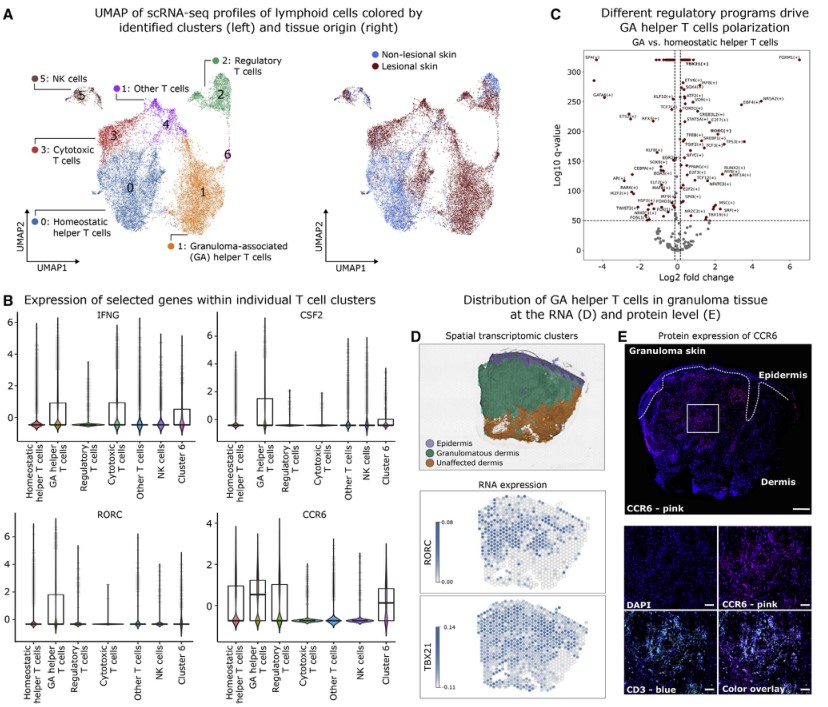
Figure 3 具有Th17.1表型的T细胞在肉芽肿中富集。
(E)皮肤肉芽肿的CCR6(粉红色;PE)、CD3(浅蓝色;AF750)和DAPI(深蓝色)的免疫荧光样本。
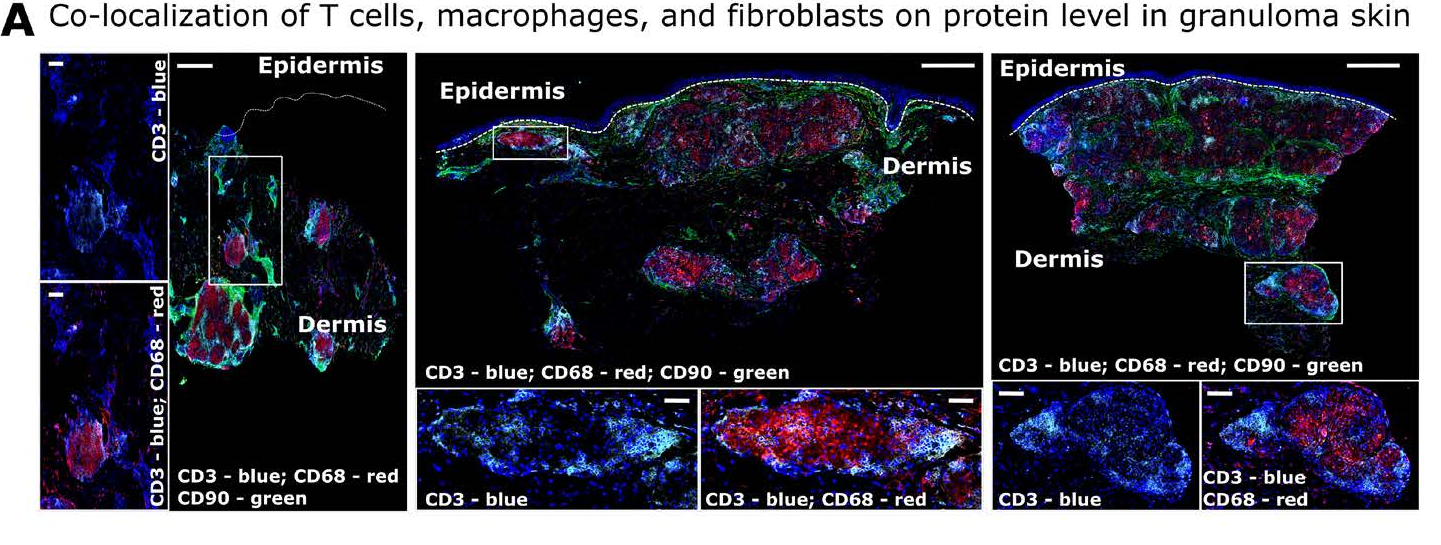
Figure S3 Th17.1细胞在肉芽肿中丰富,并与巨噬细胞相互作用。
单细胞测序鉴定了7个淋巴细胞簇。簇0的辅助T细胞包括损伤性和非损伤性皮肤细胞,而簇1的细胞主要来自损伤性皮肤(Figure 4A)。因此,我们将簇0称为稳态辅助T细胞,将簇1称为GA辅助T细胞。
GA辅助性T细胞似乎已经获得了一种慢性激活的Th17.1表型。Th17.1细胞的特征是IL-23和IL-12驱动的从Th17向Th1表型的转化。Th17.1细胞依赖于转录因子T-bet和Rorγt 的联合活性,这两种转录因子确实在GA辅助性T细胞(Figure 3C)和肉芽肿皮肤(Figure 3D)中共表达。Th17.1细胞通过CCL20-CCR6轴被招募到炎症部位,其中CCL20由髓系细胞产生,而其受体CCR6在T细胞上表达(图4B)。免疫荧光样本图像显示CD3+ T胞在肉芽肿内部表达CCR6 (Figure 3E和S3F)。免疫荧光蛋白染色鉴定了CD3+ T细胞,它们既存在于肉芽肿内,也存在于其附近(图S3A)。
结构细胞促进肉芽肿局部炎症和组织重塑
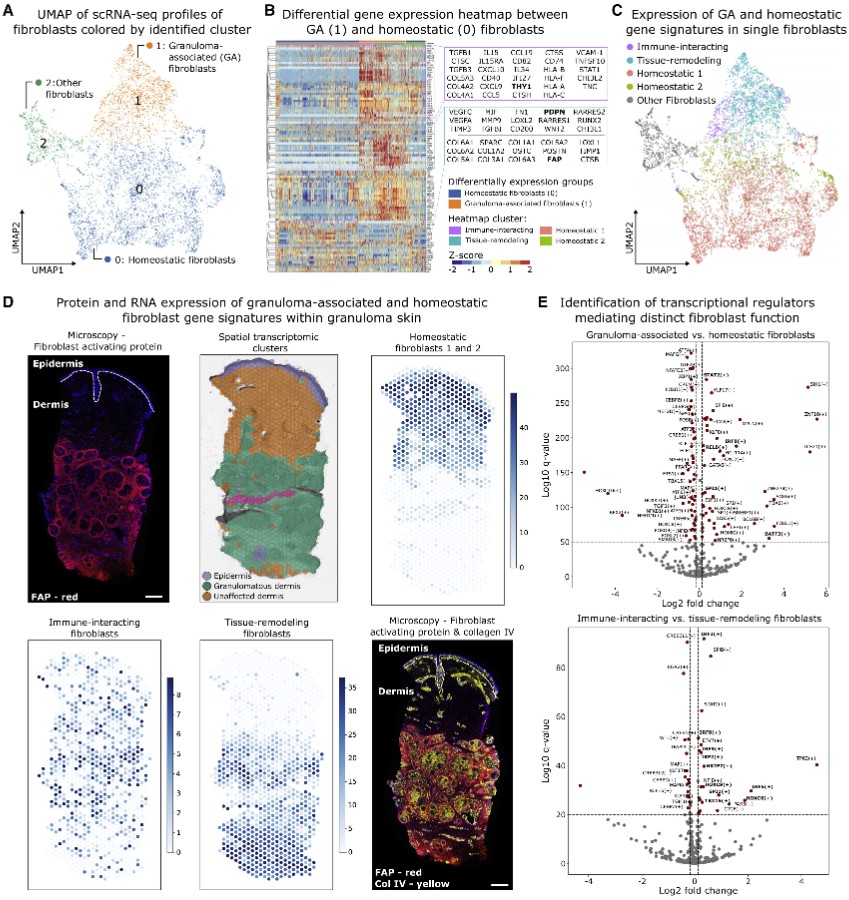
Figure 4 结构细胞促进肉芽肿局部炎症和组织重塑
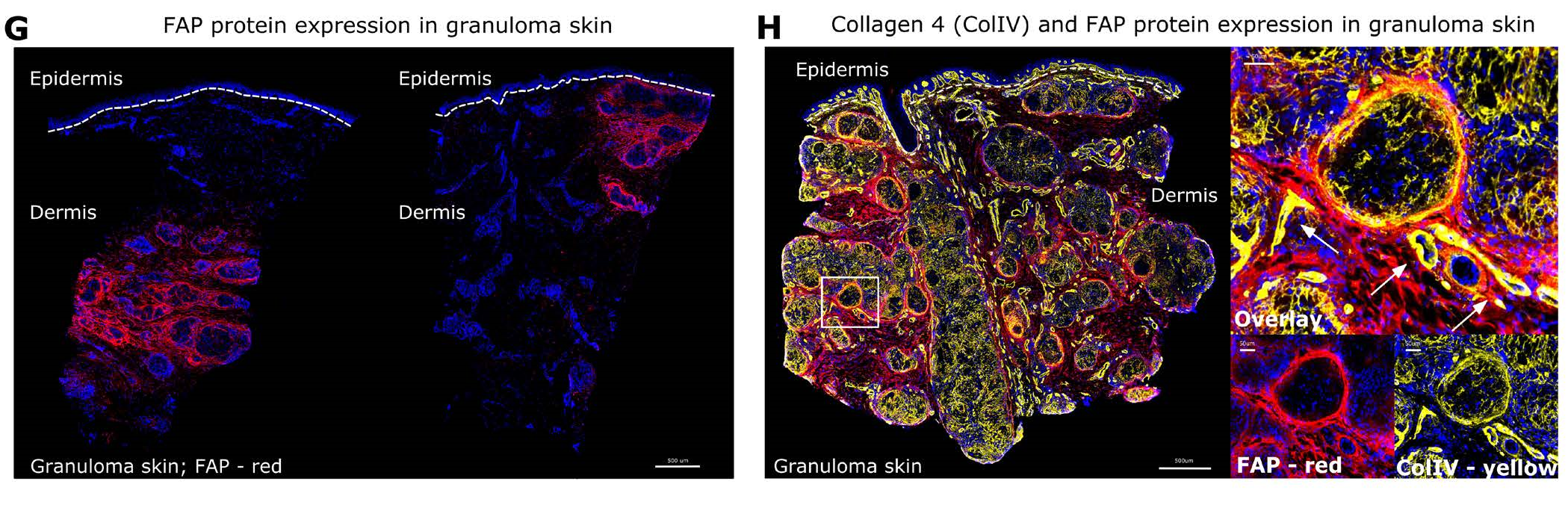
Figure S4 FAP标记GA成纤维细胞并将其定位于肉芽肿结构。
(G)皮肤肉芽肿成纤维细胞激活蛋白(FAP,红色;APC)和DAPI(深蓝)的免疫荧光染色图像。(H)皮肤肉芽肿的成纤维细胞激活蛋白(FAP,红色;APC)、IV型胶原(ColIV,黄色;PE)和DAPI(深蓝)的免疫荧光蛋白染色。白色箭头表示表达IV型胶原(ColIV)的内皮细胞。
在成纤维细胞中,我们鉴定出三个簇(Figure 4A)。簇0主要与非病变皮肤相关,簇1主要由病变皮肤组成,而簇2包含了来自两种来源的细胞(Figure S4D)。因此,我们将簇0称为“稳态成纤维细胞”,将簇1称为“GA成纤维细胞”。
在病变皮肤中,GA成纤维细胞位于肉芽肿附近,显示出高水平的炎症标志物FAP的mRNA表达(Figure 4D和S4G)。在肉芽肿外部检测到稳态成纤维细胞,而免疫相互作用成纤维细胞的基因特征在这些结构附近检测到,而组织重塑成纤维细胞主要位于肉芽肿内部,表明ECM成分是在这些发炎的结构内分泌的(Figure 4D)。ECM重塑在肉芽肿中的重要性得到了进一步的支持,因为在组织重塑成纤维细胞(Figure 4D和S4H)和肉芽肿周围的内皮细胞(Figure S4C和S4H)中高表达了IV型胶原蛋白,以及巨噬细胞特异性mRNA表达的金属蛋白酶(MMP9和MMP12),它们已知能降解包括IV型胶原蛋白在内的ECM蛋白质(Figure 4B和S4E)。基质沉积和降解的动态平衡可能促进淋巴细胞的迁移,同时增强肉芽肿内免疫细胞的粘附和保留。
免疫和结构细胞之间的细胞间互相作用定义了肉芽肿的结构
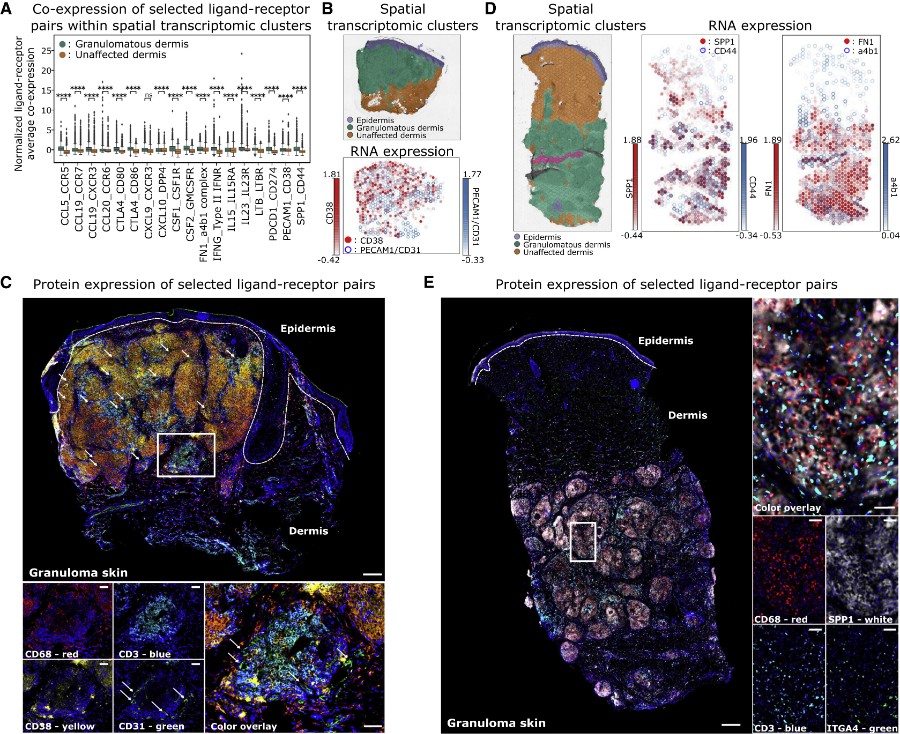
Figure 5 免疫和结构细胞之间的细胞间交流定义了肉芽肿的结构
(C) CD68 (红色; APC)、CD3 (浅蓝色; AF750)、CD38 (黄色;PE)、CD31/PECAM1 (绿色; FITC) 和DAPI (深蓝色) 对皮肤肉芽肿进行免疫荧光染色。白色箭头指示内皮细胞。
(E) CD68 (红色; APC)、CD3 (浅蓝色; PE-TR)、SPP1 (浅粉色;AF750)、ITGA4 (绿色; FITC) 和DAPI (深蓝色) 对皮肤肉芽肿进行免疫荧光染色。
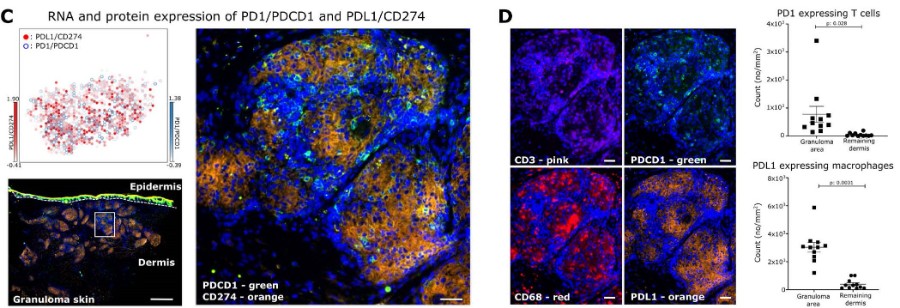
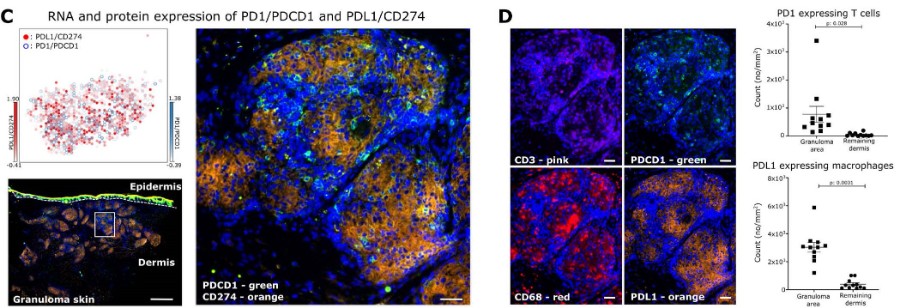
Figure S5 配体-受体相互作用定位于肉芽肿结构
(C)左上角:基于受体-配体对PDL1(CD274,红色)和PD1(PDCD1,蓝色)的空间转录数据的基因表达。左下和右下:皮肤肉芽肿的免疫荧光蛋白染色:PD1/PDCD1(绿色;FITC)、PDL1/CD274(橙色;PE-TR)和DAPI(蓝色)。
(D)皮肤肉芽肿的免疫荧光染色:PD1/PDCD1(绿色,FITC)、PDL1/CD274(橙色,PE-TR)、CD68(红色;APC)、CD3(粉红色;PE)和DAPI(深蓝色)。左图:放大与图C相同的肉芽肿结构。右图:表达PD1的T细胞(CD3+PD1+)和表达PDL1的巨噬细胞(CD68+PDL1+)的定量。
GA巨噬细胞、T细胞和成纤维细胞表达了许多趋化因子和趋化因子受体,预测了细胞间相互作用(例如,CXCR3与CXCL9、CXCL10、CXCL11和CCL19;CCR5和CCR1与CCL5;以及CCR7与CCL19)。本文还证实了前面讨论过的几种与炎症相关的相互作用(CCR6与CCL20;GMCSFR与CSF2;以及CSF1R与CSF1),这些相互作用在空间转录组数据中被观察到,并且在肉芽肿内显著富集(Figure 5A,5B, 5D )。
GA辅助T细胞表达IFNG,作用于巨噬细胞和结构细胞等表达IFNGR1的细胞(Figure 5A)。GA辅助T细胞还表达LTB,而相应的受体LTBR在巨噬细胞、成纤维细胞和内皮细胞中表达(Figure 5A)。在淋巴器官形成过程中,LTB导致成纤维细胞分泌VEGF-C,促进内皮细胞发育并诱导内皮细胞上的粘附分子的表达。在内皮细胞中检测到PECAM1的表达,它预测了与肉芽肿中GA巨噬细胞和GA辅助T细胞的相互作用,这种相互作用被免疫荧光蛋白染色证实(Figure 5B-C)。
在肉芽肿内观察到PDCD1和CD274的高表达(Figure 5A),并通过免疫荧光蛋白染色确认了相应蛋白的共定位(Figure S5C)。肉芽肿中PD1表达的T细胞和PD-L1表达的巨噬细胞增加,与非炎症性皮肤相比(Figure S5D),这可能随着时间的推移导致肉芽肿内T细胞的耗竭。最后,IL23和IL23R在肉芽肿中也高表达,可能有助于创造一个有利于Th17.1细胞表型的细胞环境。
该数据预测了肉芽肿内巨噬细胞、T细胞和结构细胞之间的密集的细胞-细胞相互作用网络,这可能有助于促进炎症环境和吸引和保留驱动结节病病理的免疫细胞。
肉芽肿与TLSs具有关键的共同特征
本文建立了一个12种趋化因子的TLS基因特征,发现它在肉芽肿中高度表达。具体来说,CCL5、CXCL9和CXCL10在GA巨噬细胞中上调,CCL4和CCL5在GA T细胞中上调,CCL5、CCL19、CXCL9、CXCL10以及CXCL11在GA成纤维细胞中上调。我们还观察到肉芽肿特异性的CCL19-CCR7/CXCR3通路的活性,该通路涉及T细胞回归淋巴器官。这些结果表明,肉芽肿利用了一些与TLS形成相关的相同的生物学过程。
扩展阅读
在本文中,研究者大量使用单细胞测序技术和原位空间转录组技术,以确定不同细胞表型及其原位分布规律,但是现阶段原位空间转录组技术仍然无法达到单细胞分辨率下的作用关系分析,同时单一技术仍然无法解决转录组数据和蛋白组数据的相互验证。Tissue Cytometry技术作为当前组织原位单细胞定量分析的标准之一,无论是在鉴别多荧光标记样本中不同蛋白表型单细胞,或是对其单细胞蛋白表达进行定量分析,或是根据需要识别定量不同的组织类型,或是评估单细胞或组织的相互作用关系等应用领域,均可以提供完善的解决方案。本文作者通过这两种技术互为依托补充,相互验证,使研究的可靠性和精准性得到了坚实的基础。
近年来,随着对组织原位结构微环境的解析研究不断深入,TissueGnostics公司提出了”肿瘤亚微环境“的理念,通过解析肿瘤”癌岛“之间的细胞构成模式,探索在细胞聚类结构中新型免疫作用中心的构成极其意义。在这个探索中,全球顶级实验室的多位研究者陆续发表了肿瘤三级淋巴结构相关研究,肿瘤基质与肿瘤血管的相互作用研究等多篇论文。本文研究者也提出,通过研究证实肉芽肿在一定程度上和TLS具有相似性。相信不久以后也会有更多的研究,在利用Tissue Cytometry技术拓展未来的研究方向。