肝癌,作为全球范围内的重大健康挑战,其发病机制一直是科学界努力探索的焦点。肿瘤微环境(TME)在肝癌的发生发展中扮演着关键角色,其中癌相关成纤维细胞(CAF)更是备受瞩目。
肿瘤生长依赖肿瘤微环境(TME),其中癌相关成纤维细胞(CAF)起重要作用,已鉴定出多种 CAF 亚型。原发性肝癌(PLC)预后差,肝癌中 CAF 主要源于肝星状细胞,且有多种亚型调控肿瘤进展。尽管单细胞 RNA 测序提供了 CAF 信息,但空间技术的出现使人们能更直观研究 TME 多成分协调机制,不过某些 CAF 表型的空间邻域及功能变化仍不清楚。

近日,东方肝胆医院外科研究所王红阳院士团队在Genome Medicine发表题为“Spatial multiomics reveals a subpopulation of fibroblasts associated with cancer stemness in human hepatocellular carcinoma”的文章利用空间多组学技术,对人肝癌样本进行分析,揭示了肿瘤微环境中基质组织,尤其是成纤维细胞的作用,鉴定出一种与癌症干性和不良预后相关的癌相关成纤维细胞(CAF)亚群 F5-CAF。此项研究对于揭示肝癌发病机制、开发有效治疗策略至关重要。
研究团队为深入探究肝癌相关机制,运用基于质谱的蛋白质组学明确差异表达蛋白;而后通过开展空间转录组学实验来分析基因表达;在成纤维细胞研究方面,综合 ST 和 scRNA - seq 数据重新聚类鉴定出 F5 - CAF 亚群并研究其特性。特别是在分析 F5 - CAF 与其他细胞关系时,采用多重免疫荧光染色结合TissueFAXS Spetcra 全景多光谱扫描定量分析系统,使用 StrataQuest 软件,利用光谱库拆分、DAPI 细胞核分割、组织分割算法等排除干扰,有效验证空间转录组结果,从多方面为研究提供有力支持。
实验部分
作者借助Tissue Cytometry技术,使用多重免疫荧光染色方法实现了对肝细胞癌组织中多个标记物(EPCAM、COL4A2、CTGF、FSTL1和COL1A2)的同时检测,这对于揭示肿瘤微环境中的细胞相互作用至关重要。在成像方面,Tissue Cytometry技术通过光谱拆分算法有效区分了不同荧光标记物的信号,减少了交叉荧光干扰,提高了信号识别的准确性。
在分析方面,Tissue Cytometry技术的使用让DAPI染色的细胞核的识别和分割更加精确,尤其是在复杂的组织切片中可以更准确定位特定细胞群体。在下一步中,Tissue Cytometry组织分割算法的应用,进一步精确划分了不同类型的组织区域,为细胞类型筛选和功能作用分析提供了便利。
在本文中Tissue Cytometry多层级分析技术的综合应用,不仅提高了数据分析的效率和准确性,还为评估F5-CAFs与患者预后的相关性提供了强有力的工具,对癌症研究和临床治疗策略的开发具有重要的意义。
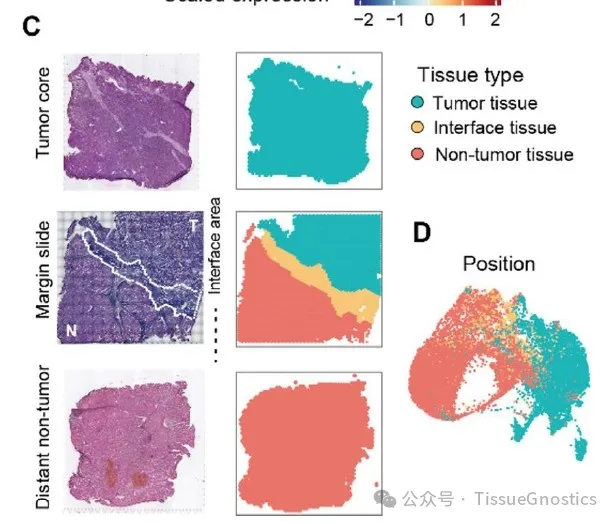
Figure 1 通过 ST 分析揭示成纤维细胞的功能多样性和异质性。
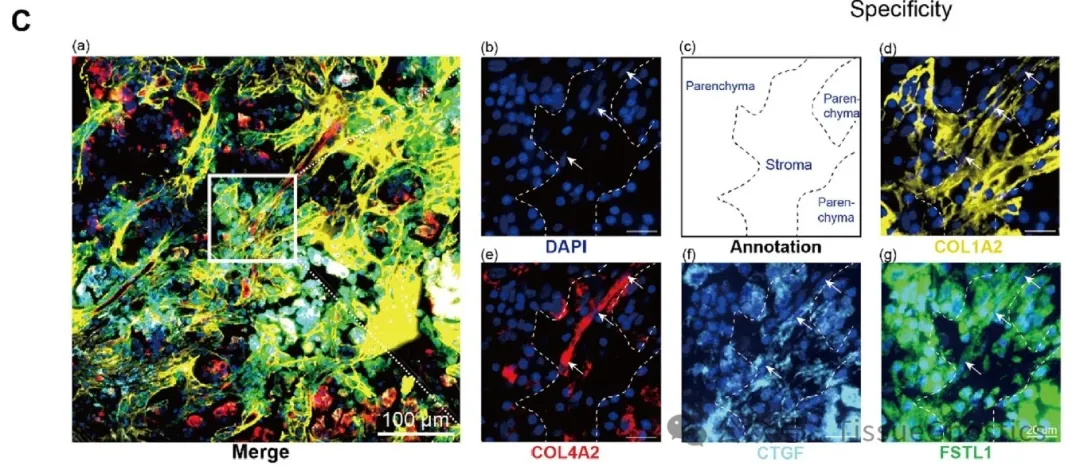
Figure 2 肝癌患者中的 F5-CAFs 与预后不良有关。
(C)肿瘤核心组织的多重免疫荧光图像。c,实质组织和基质组织位置的注释图;d-g,显示每个标记物,以及 DAPI 核标记物和自发荧光信号。白色箭头所指的纺锤形细胞是成纤维细胞,五种标记物均呈阳性。
Tissue Cytometry技术准确识别了不同细胞类型的空间位置,明确了 F5-CAF 与其他细胞的共定位情况,从细胞定位、共定位以及细胞状态与功能关联等多方面对空间转录组结果进行了有效验证,为研究结论提供了可靠的证据支持。
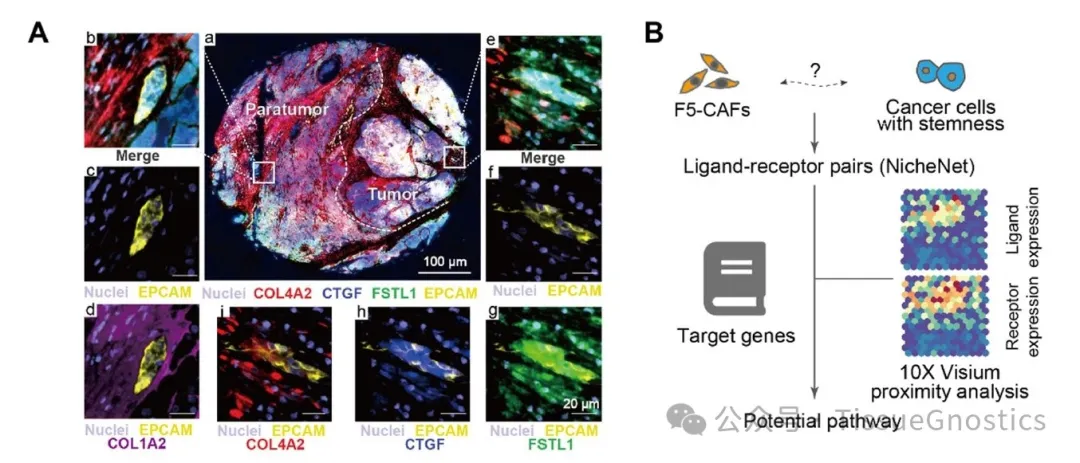
Figure 3 F5-CAFs 与 HCC CSCs 之间的细胞串联。
(A) HCC 界面区域的多重免疫荧光图像。a,合并图像。虚线表示肿瘤组织的边界。b-i,非肿瘤区(b-d)或肿瘤区(e-i)的放大图像,显示五个合并标记物(b、e)或肿瘤区(e-i)。
本研究通过空间多组学分析全面揭示了肝癌 TME 中肿瘤基质和 CAF 的特性,鉴定出的 F5-CAF 亚群为肝癌研究提供了新的靶点和方向。未来,有望基于这些发现开发出更精准有效的肝癌治疗策略,为改善肝癌患者的预后带来新的希望。同时,Tissue Cytometry技术在本研究中的成功应用,也为相关领域的研究提供了有力的技术支持范例,发挥了重要的作用。
这项研究不仅加深了我们对肝癌发病机制的理解,更为肝癌的治疗提供了新的思路和潜在靶点。期待未来能有更多的研究成果转化为临床应用,造福广大肝癌患者。